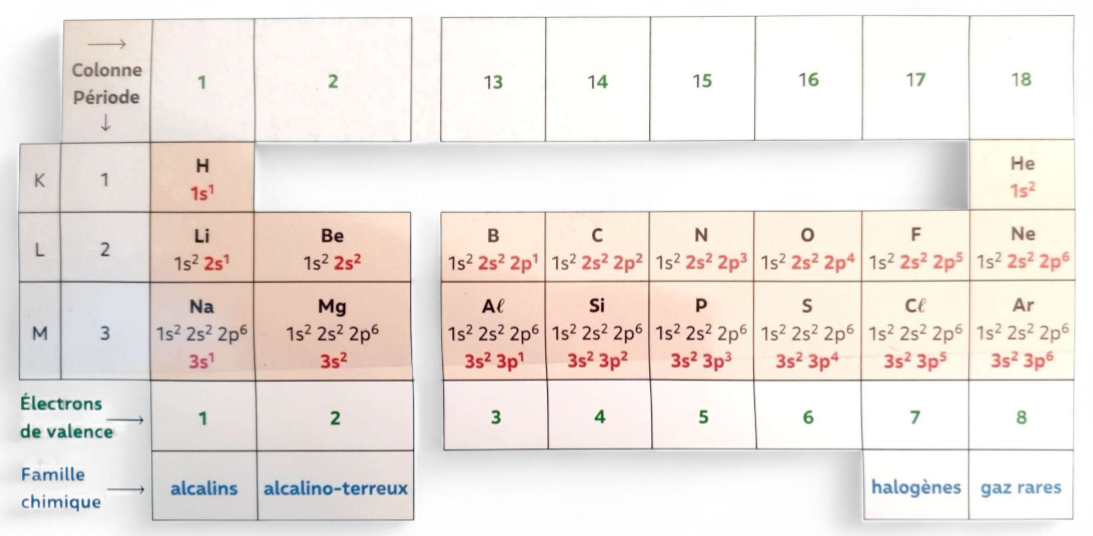
8. Lien avec la classification périodique
La position dépend de la configuration électronique.
- Ligne (période) = nombre de couches
- Colonne (famille) = électrons de valence
Sodium : 2 / 8 / 1
- 3 couches → période 3
- 1 électron externe → colonne 1
L’atome est constitué :
👉 Les électrons sont organisés en couches électroniques et en sous-couches.
👉 On remplit toujours dans l’ordre : K → L → M
Méthode :
Sodium (Z = 11)
→ 2 / 8 / 1
Les électrons occupent des orbitales appelées :
Carbone (Z = 6)
1s² 2s² 2p²
👉 Explication :
Silicium (Z = 14)
1s² 2s² 2p⁶ 3s² 3p²
👉 Pourquoi 3s² 3p² ?
Les électrons de valence sont ceux de la couche externe.
Carbone : 2s² 2p² → 4 électrons de valence
Silicium : 3s² 3p² → 4 électrons de valence
👉 Ce sont eux qui déterminent les propriétés chimiques.
👉 Les gaz nobles sont stables (couche remplie)
Un atome devient stable en :
Sodium : 2 / 8 / 1 → perd 1 → Na⁺
Chlore : 2 / 8 / 7 → gagne 1 → Cl⁻
La position dépend de la configuration électronique.
Sodium : 2 / 8 / 1

Les éléments d’une même colonne ont :
Famille du carbone → 4 électrons externes
Aluminium (Z = 13)
Configuration :
1s² 2s² 2p⁶ 3s² 3p¹